44款化药2.4类新药获批上市!360多家企业布局,恒瑞医药领跑! 改良型新药因较创新药研发耗资少、耗时短、风险低和回报可观且受到政策支持而越来越受到我国药企重视。化药2.4类,是指含有已... |
您所在的位置:网站首页 › 电动车 一公里多少钱 › 44款化药2.4类新药获批上市!360多家企业布局,恒瑞医药领跑! 改良型新药因较创新药研发耗资少、耗时短、风险低和回报可观且受到政策支持而越来越受到我国药企重视。化药2.4类,是指含有已... |
44款化药2.4类新药获批上市!360多家企业布局,恒瑞医药领跑! 改良型新药因较创新药研发耗资少、耗时短、风险低和回报可观且受到政策支持而越来越受到我国药企重视。化药2.4类,是指含有已...
|
来源:雪球App,作者: 药融云医药大数据,(https://xueqiu.com/1883007513/259833317) 
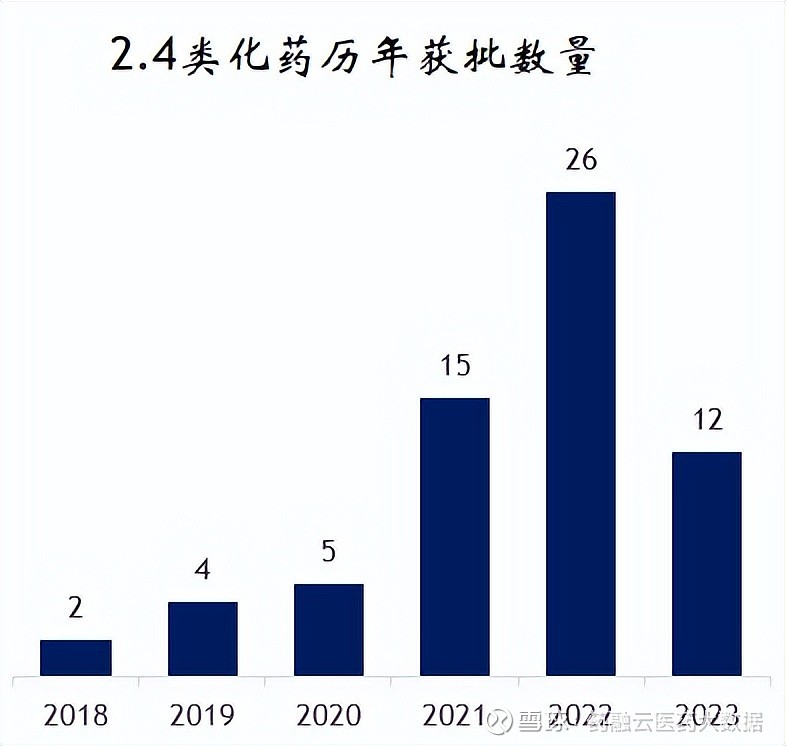
改良型新药因较创新药研发耗资少、耗时短、风险低和回报可观且受到政策支持而越来越受到我国药企重视。化药2.4类,是指含有已知活性成份的新适应症的制剂,同样也是国内对2类改良新药重要的开发方向之一。 360多家企业布局化药2.4类新药!抗肿瘤药物占比近一半据药融云《改良型新药全景展示》报告统计,截至2023年7月21日,CDE公示的化药改良型新药受理号共计1906个,其中2.4类(新适应症)的有1069个,占比37%,涉及250个品种,362家企业。 从申请类型分布看,2.4类以进口药物偏多;从治疗领域分布看,受理号治疗领域集中在抗肿瘤药和免疫机能调节药、消化系统与代谢药、抗感染药和血液和神经系统用药,分布占比46%、10%、9%、7%。 药融云数据库显示,截至2023年7月21日,已获批上市的化药2.4类品种共计44个,仅2022年就获批26个品种,创历史新高;涉及$恒瑞医药(SH600276)$ 、$百济神州(06160)$ 、$贝达药业(SZ300558)$ 、豪森药业、国药集团、健康元、人福药业、海思科等多家药企。(注:同一年份同一品种不同获批时间算多个) 化药2.4类历年获批数量
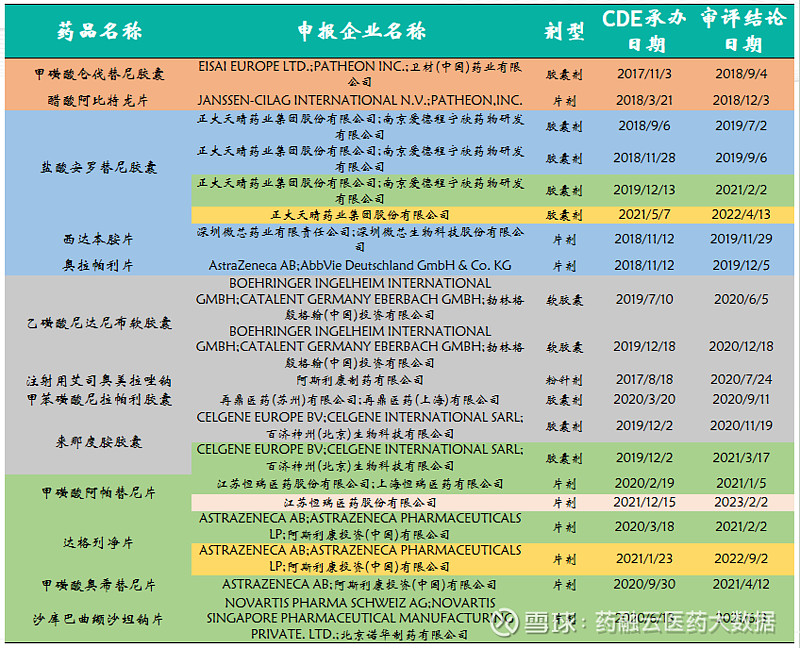
数据来源:药融云中国药品审评数据库 44款2.4类新药获批上市!恒瑞医药领跑从企业获批数量来看,恒瑞医药收获最多为5款,包括甲磺酸阿帕替尼片、注射用甲苯磺酸瑞马唑仑、马来酸吡咯替尼片、羟乙磺酸达尔西利片、氟唑帕利胶囊;其次为阿斯利康有4款获批(注射用艾司奥美拉唑钠、甲磺酸奥希替尼片、奥拉帕利片、达格列净片),拜耳有4款获批(利伐沙班片、利伐沙班颗粒、非奈利酮片、达罗他胺片),百济神州有2款获批(来那度胺胶囊、泽布替尼胶囊)等等。 获批上市的2.4类新药(部分)
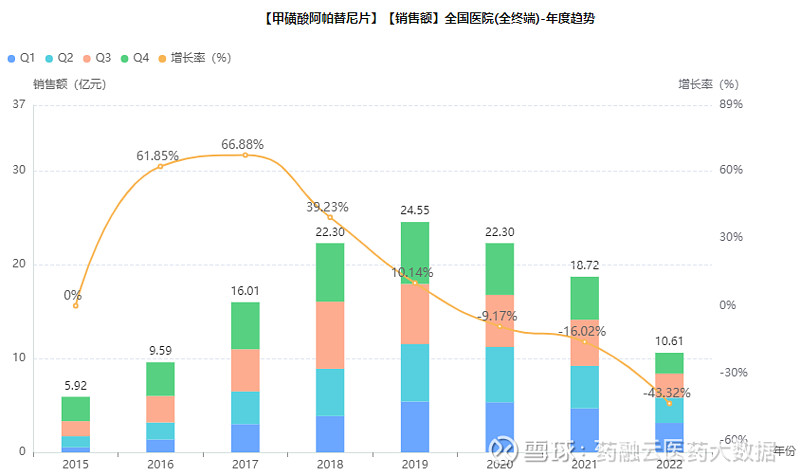
图片来源:药融云《改良型新药全景展示》报告 甲磺酸阿帕替尼片(受理号:CXHS2101056)获批的新适应症,是联合注射用卡瑞利珠单抗用于不可切除或转移性肝细胞癌患者的一线治疗。甲磺酸阿帕替尼片是恒瑞医药历时10年研发的具有自主知识产权的小分子抗血管生成靶向药物,于2014年获批上市,2017年进入国家医保目录。 药融云全国医院销售(全终端)数据库显示,甲磺酸阿帕替尼片上市后的五年时间在医院终端市场的销售规模处于大幅上涨的态势,增长率最高为66.88%,2019年医院端的销售额达到24.55亿元;2020年后销售规模呈现下降趋势。
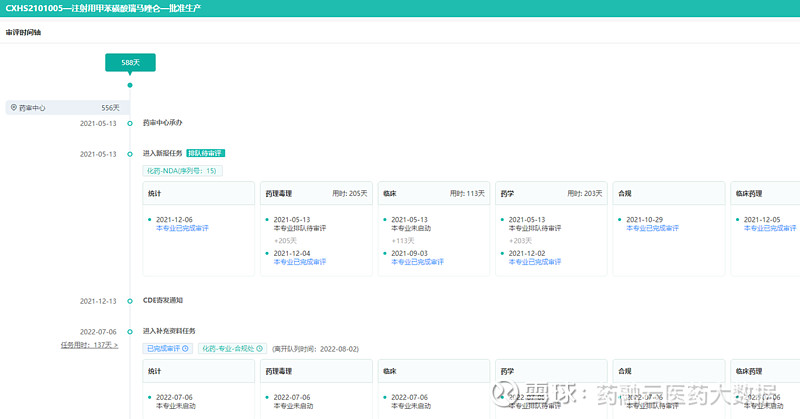
图片来源:药融云全国医院销售(全终端)数据库 注射用甲苯磺酸瑞马唑仑(商品名:瑞倍宁)属于苯二氮䓬类药物,是一种新型的短效GABAa受体激动剂,它通过全身血浆酯酶代谢,并且代谢产物无活性,具有起效迅速、苏醒快、对心血管和呼吸系统影响小、以及具有镇静逆转剂等优点。 药融云数据库显示,注射用甲苯磺酸瑞马唑仑已获批多项适应症,2019年12月首个适应症获批,用于胃镜检查镇静;2020年6月第二个适应症获批上市,用于结肠镜诊疗镇静;2021年11 月再次获批新适应症,用于全身麻醉的诱导和维持;2022年12月获批第四个适应症,用于支气管镜诊疗麻醉。 注射用甲苯磺酸瑞马唑仑新适应症获批耗时588天
图片来源:药融云中国药品审评数据库 随着新适应症陆续获批,注射用甲苯磺酸瑞马唑仑在全国医院终端市场的销售规模也在不断扩大,2022年的销售额为1.68亿元,同比增长10.37%。 马来酸吡咯替尼片(商品名:艾瑞妮)是一种不可逆性HER2、表皮生长因子受体(EGFR)双靶点酪氨酸激酶抑制剂,通过阻止表皮生长因子受体(HER)家族(EGFR、HER2、HER3和HER4)信号通路转导,达到抗癌目的,用于治疗复发或转移性乳腺癌。于2018年8月获国家药监局有条件批准上市,并于2020年7月获得完全批准。 于2022年6月获批新适应症,与曲妥珠单抗和多西他赛联合,用于表皮生长因子受体 2(HER2)阳性早期或局部晚期乳腺癌患者的新辅助治疗。后于2023年4月又获批新适应症。 马来酸吡咯替尼片新适应症获批耗时194天
图片来源:药融云中国药品审评数据库 据药融云中国药品审评数据库统计,已获批上市的化药2.4类品种平均审评时长为359天,中位数321天,最短175天,最长1071天。 国产1类新药上市后,伴随着2类改良新药的注册申报,已从一种趋势变为一种常态,以期获得更大的临床使用范围及适应症市场。通过药融云数据库统计不难发现,近年来2类新药的注册申报数量明显增多,其中2.2类和2.4类是最主要的类型。未来,2类新药的注册申报必会成为更为聚集的热点方向。 |
【本文地址】